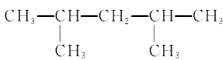 ,
,
该烯烃可能有的结构数目是( )




①气体的颜色________
②试管中的液面________,
③试管中有________和________出现,
④水槽中还观察到________.
此反应中产物一共有________种,其中物质的量最多的是________.
写出上述反应的有关化学反应方程式:________.


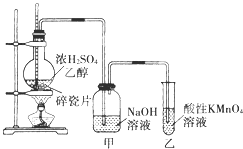
②在各装置中注入相应的试剂(如图所示);
③点燃酒精灯加热;实验时,烧瓶中液体混合物逐渐变黑.

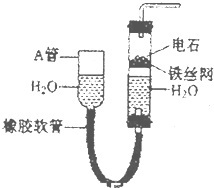

![]()
反应①的化学方程式是_________,
反应类型为_________,反应②的反应类型为_________。

已知相关燃烧热数据:
C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) △H1=-1411kJ·mol-1
C3H6(g)+  O2(g)=3CO2(g)+3H2O(l) △H2=-2049kJ·mol-1
O2(g)=3CO2(g)+3H2O(l) △H2=-2049kJ·mol-1
C4H8(g)+6O2(g)=4CO2(g)+4H2O(l) △H3=-2539kJ·mol-1
①乙烯的电子式为_________。
②相同质量的C2H4(g)、C3H6(g)和C4H8(g)充分燃烧,放出的热量由多到少的顺序依次为_________(填写化学式)。
③ 上述“烯烃歧化法”的反应的热化学方程式为_________。
反应如下:主反应:3C4H8  4C3H6;副反应:C4H8
4C3H6;副反应:C4H8  2C2H4
2C2H4
测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:

①平衡体系中的丙烯和乙烯的质量比[  ]是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是_________(填字母序号)
]是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是_________(填字母序号)
A. 300℃ 0.1MPa B. 700℃ 0.1MPa
C.300℃ 0.5MPa D.700℃ 0.5MPa
②有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原理角度分析其理由可能是_________。
③图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是_________。