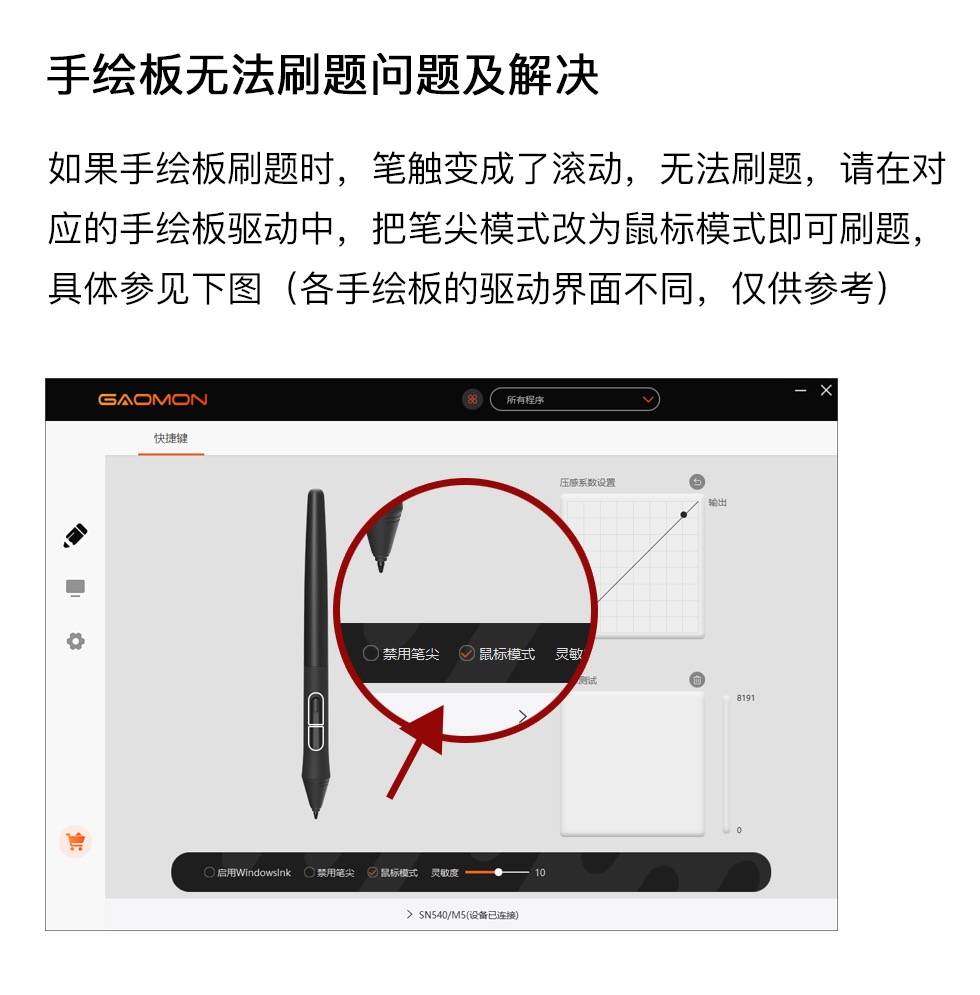
北京版化学九年级下册第11章 酸与碱第一节 对酸碱的初步认识同步测试
一、选择题
推理是学化学的一种重要方法,但不合理的推理会得出错误结论。以下推理正确的是
A.
分子可以构成物质,物质一定是由分子构成的
B.
离子是带电荷的微粒,带电荷的微粒一定是离子
C.
碱溶液的pH都大于7,pH大于7的溶液一定是碱溶液
D.
含碳元素的物质充分燃烧会生成CO2,燃烧能生成CO2的物质一定含碳元素

我要多选
作答:
答对了
答错了
常温下,一些食物的近似pH如下表所示,下列说法中,正确的是
| 食物 | 苹果汁 | 牛奶 | 鸡蛋清 | 红豆汁 |
| pH | 2.9 | 6.3 | 7.6 | 10.2 |
A.
牛奶放置一段时间后变酸,pH变大
B.
红豆汁能使紫色石蕊试液变红
C.
牛奶和鸡蛋清都显碱性
D.
胃酸过多的人应该少饮苹果汁

我要多选
作答:
答对了
答错了
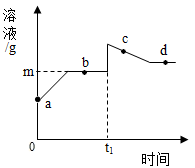
向盛有一定溶质质量分数稀硫酸的烧杯中加入一定量的铁粉,充分反应后,在t1时刻迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列选项正确的是

A.
a→b点,溶液的pH逐渐减小
B.
向b点所得溶液中加入镁,会产生大量气泡
C.
c点时,溶液中有两种溶质
D.
向d点固体中滴加稀盐酸一定有气泡产生

我要多选
作答:
答对了
答错了
下列有关实验现象的描述正确的是
A.
一氧化碳在空气中燃烧火焰呈蓝色,放出大量的热
B.
向足量的铁粉中加入硫酸铜溶液,充分反应后,观察到溶液由浅绿色变为蓝色
C.
向pH=4的无色溶液中滴入2滴石蕊溶液,溶液由紫色变为蓝色
D.
红磷在空气中燃烧,产生大量白色烟雾

我要多选
作答:
答对了
答错了
某同学对化学课本上几个实验结果的分析正确的是
A.
测定空气中氧气含量,实验前弹簧夹未夹紧,测得结果比实际值偏大
B.
用湿润的pH试纸测定氢氧化钠溶液的pH,测得结果比实际值偏大
C.
配好的氯化钠溶液转移至细口瓶时有洒落,测得结果比实际值偏小
D.
粗盐提纯实验中,蒸发时液滴飞溅,测得的产率与实际值一样

我要多选
作答:
答对了
答错了
依据下列实验现象得出的结论,正确的是
| 选项 | 实验现象 | 结论 |
| A | 某溶液的pH大于7 | 该溶液一定是碱溶液 |
| B | 某金属与盐酸反应比铝与硫酸反应剧烈 | 该金属的活动性比铝的强 |
| C | 某无色溶液中滴加紫色石蕊试液,呈红色 | 该无色溶液显酸性 |
| D | 某水样中滴加肥皂水后振荡,产生大量泡沫 | 该水样属于硬水 |
A.
A
B.
B
C.
C
D.
D

我要多选
作答:
答对了
答错了
取稀盐酸与氢氧化钠反应后的溶液进行实验。下列实验能说明稀盐酸、氢氧化钠恰好完全反应的是
A.
加硝酸银溶液,有白色沉淀生成
B.
加氢氧化镁固体,固体全部溶解
C.
加酚酞试液,溶液显红色
D.
测定溶液的pH,pH=7

我要多选
作答:
答对了
答错了
下列实验方案能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去FeCl2溶液中少量的CuCl2 | 加入足量铁粉,过滤 |
| B | 除去CO2气体中少量的HCl气体 | 通过NaOH溶液 |
| C | 探究稀盐酸和NaOH溶液是否完全反应 | 向反应后的溶液中加入AgNO3溶液 |
| D | 鉴别木炭粉和氧化铜粉末 |

我要多选
作答:
答对了
答错了
下列图象能正确反应对应变化的是_____
| A | 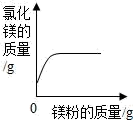 | 向一定质量的盐酸中加入镁粉至过量 |
| B | 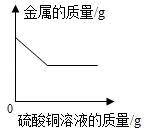 | 向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 |
| C | 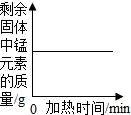 | 加热一定量的高锰酸钾固体 |
| D | 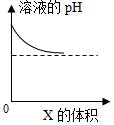 | 向氢氧化钠溶液中加入 X,X 可能是 |

我要多选
作答:
答对了
答错了
向一无色溶液中滴加数滴酚酞溶液,溶液变红,该无色溶液可能是( )
A. 氯化钠溶液 B. 稀盐酸 C. 澄清石灰水 D.________________
A. 氯化钠溶液 B. 稀盐酸 C. 澄清石灰水 D.

我要多选
作答:
答对了
答错了
二、判断题
pH试纸用蒸馏水润湿后测得溶液pH偏小。( )

我要多选
作答:
答对了
答错了
碱溶液能使石蕊变蓝,能使石蕊变蓝的一定是碱。( )

我要多选
作答:
答对了
答错了
用广泛pH试纸测得溶液的pH为3.5。( )

我要多选
作答:
答对了
答错了
用pH试纸测定白醋的酸碱度时,先将试纸用蒸馏水润湿,再把白醋滴在试纸上。( )

我要多选
作答:
答对了
答错了
三、填空题
做没有明显现象发生的中和反应时,需要用到酸碱指示剂,这种指示剂是_______ 。

我要多选
作答:
答对了
答错了
液体药品的取用
(1)较多量:倾倒法,瓶塞倒放,标签靠手心,瓶口______ 容器口。
(2)较少量:用胶头滴管滴加,注意要“_______ ”。
(3)极少量:用pH试纸测液体的pH时,应用_______ 蘸取待测液沾到pH试纸上,观察颜色。
(1)较多量:倾倒法,瓶塞倒放,标签靠手心,瓶口
(2)较少量:用胶头滴管滴加,注意要“
(3)极少量:用pH试纸测液体的pH时,应用

我要多选
作答:
答对了
答错了
在实验室用15 mL氢氧化钠稀溶液和稀盐酸进行中和反应实验。回答下列问题:
(1)完成该实验必须使用的仪器是:_____________
(2)要判断氢氧化钠恰好被盐酸中和,需要加入___________ 试剂,观察到的现象是___________
(3)要从中和后的溶液中获取氯化钠晶体,应进行的操作是:__________ 。
(1)完成该实验必须使用的仪器是:
(2)要判断氢氧化钠恰好被盐酸中和,需要加入
(3)要从中和后的溶液中获取氯化钠晶体,应进行的操作是:

我要多选
作答:
答对了
答错了
请选择符合题意的物质,用字母填空。
A.酚酞试液 B.铁 C.氧气 D.酒精 E.二氧化碳
(1)能供给人体呼吸的是___________ 。
(2)属于酸碱指示剂的是___________ 。
(3)实验室常用的燃料是___________ 。
(4)常见的金属是___________ 。
(5)能产生温室效应的气体是___________ 。
A.酚酞试液 B.铁 C.氧气 D.酒精 E.二氧化碳
(1)能供给人体呼吸的是
(2)属于酸碱指示剂的是
(3)实验室常用的燃料是
(4)常见的金属是
(5)能产生温室效应的气体是

我要多选
作答:
答对了
答错了
在用稀盐酸和氢氧化钠探究酸与碱的中和反应时,小梅先在烧杯中加入5 mLA溶液,再用胶头滴管慢慢滴入B溶液,并不断搅拌溶液,同时用pH传感器测得溶液的pH变化如图所示。请根据图像回答下列问题:
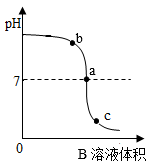
(1)A溶液为________ 溶液。
(2)盐酸与氢氧化钠恰好完全反应的点为________ (选填“a”“b”或“c”)点。
(3)向c点溶液中滴加紫色石蕊溶液,溶液显________ 色。

(1)A溶液为
(2)盐酸与氢氧化钠恰好完全反应的点为
(3)向c点溶液中滴加紫色石蕊溶液,溶液显

我要多选
作答:
答对了
答错了
四、简答题
自然界并不缺少“镁”,而是缺少发现“镁”的眼睛。某化学兴趣小组开启寻“镁”之旅。
(1)镁是一种__________ 色的固体,质软,有导电性。
(2)将2根打磨光亮的镁条分别放入等质量、等质量分数的稀盐酸和稀硫酸中,充分反应后镁条有剩余,产生氢气的质量 。(3)探究金属镁的性质
【提出问题】镁与水是否发生反应?反应后的生成物是什么?
【查阅资料】70℃时Mg(OH)2在水中的溶解度很小,但溶于水的部分可以完全解离出Mg2+和OH-。
【实验步骤】
①将打磨光亮的镁条放入盛有70℃水的试管中,发现镁条表面有气泡产生。将收集的气体点燃,产生淡蓝色火焰,证明该气体为__________ 。
②向反应后的溶液中立即滴入2滴无色酚酞溶液,观察到镁条附近溶液__________ ,证明溶液中生成OH-。
【交流讨论】
③根据上述实验,写出镁与热水反应的化学方程式____________ 。
【拓展探究】
同学们又探究温度对镁与水反应速率的影响,实验数据记录如下:
④根据表中数据,分析温度对镁与水反应速率的影响是_________ 。
⑤一段时间后,同学们观察到镁条表面不再有气泡产生,镁条表面失去光泽。但将表面失去光泽的镁条打磨后再次放入热水中,发现又有气泡产生,说明镁与水反应变缓慢直至停止的可能原因是__________ 。
(1)镁是一种
(2)将2根打磨光亮的镁条分别放入等质量、等质量分数的稀盐酸和稀硫酸中,充分反应后镁条有剩余,产生氢气的质量 。(3)探究金属镁的性质
【提出问题】镁与水是否发生反应?反应后的生成物是什么?
【查阅资料】70℃时Mg(OH)2在水中的溶解度很小,但溶于水的部分可以完全解离出Mg2+和OH-。
【实验步骤】
①将打磨光亮的镁条放入盛有70℃水的试管中,发现镁条表面有气泡产生。将收集的气体点燃,产生淡蓝色火焰,证明该气体为
②向反应后的溶液中立即滴入2滴无色酚酞溶液,观察到镁条附近溶液
【交流讨论】
③根据上述实验,写出镁与热水反应的化学方程式
【拓展探究】
同学们又探究温度对镁与水反应速率的影响,实验数据记录如下:
| 反应温度(℃) | 20 | 55 | 60 | 65 | 70 |
| 收集50mL气体所用时间(s) | 295 | 257 | 196 | 124 | 74 |
④根据表中数据,分析温度对镁与水反应速率的影响是
⑤一段时间后,同学们观察到镁条表面不再有气泡产生,镁条表面失去光泽。但将表面失去光泽的镁条打磨后再次放入热水中,发现又有气泡产生,说明镁与水反应变缓慢直至停止的可能原因是
A.
相等
B.
无法判断
C.
与稀盐酸反应放出的氢气多
D.
与稀硫酸反应放出的氢气多

我要多选
作答:
答对了
答错了
人类文明进步与金属材料的关系十分密切。某课外兴趣小组探究金属镁的化学性质。
①用等质量相同表面积的打磨擦去氧化膜的镁条,分别与等体积不同浓度的稀盐酸,在一定条件下反应,实验结果如图1所示。对比a、b曲线,引起a曲线压强迅速增大的因素可能有______ 。
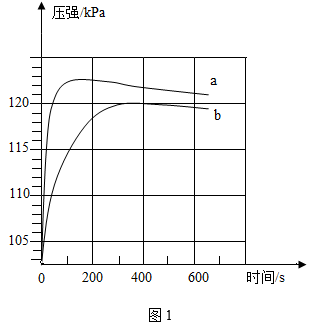

②将没有擦去氧化膜的镁条和某浓度的CuCl2溶液混合,观察到如下现象:镁条表面析出较多的紫红色固体,产生大量无色无味气体,过程中产生蓝色沉淀,同时测得反应体系溶液的pH变化曲线如图所示。下列说法错误的是__________ (填字母)。
A.实验中氧化膜能与该溶液体系反应 B.镁条表面析出紫红色固体为金属铜
C.产生的无色无味气体不可能是氢气 D.产生蓝色沉淀可能是氢氧化铜固体
①用等质量相同表面积的打磨擦去氧化膜的镁条,分别与等体积不同浓度的稀盐酸,在一定条件下反应,实验结果如图1所示。对比a、b曲线,引起a曲线压强迅速增大的因素可能有


②将没有擦去氧化膜的镁条和某浓度的CuCl2溶液混合,观察到如下现象:镁条表面析出较多的紫红色固体,产生大量无色无味气体,过程中产生蓝色沉淀,同时测得反应体系溶液的pH变化曲线如图所示。下列说法错误的是
A.实验中氧化膜能与该溶液体系反应 B.镁条表面析出紫红色固体为金属铜
C.产生的无色无味气体不可能是氢气 D.产生蓝色沉淀可能是氢氧化铜固体

我要多选
作答:
答对了
答错了
如图所示,A、B试管中各有一团用无色酚酞溶液润湿过的棉花,先关闭止水夹,将少量浓氨水滴在A试管的棉花上,然后再打开止水夹。
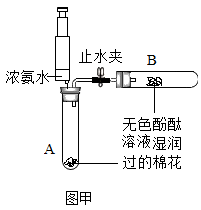
(1)请叙述A、B两处的实验现象。
(2)请用分子的观点解释B处颜色变化的原因。
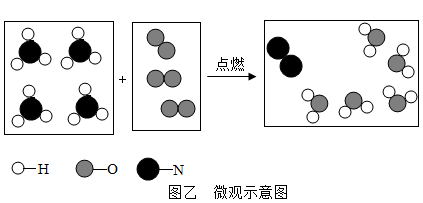
(3)氨气在纯氧中燃烧的化学方程式是 。把图乙中第三个方框补充完整。
。把图乙中第三个方框补充完整。


(1)请叙述A、B两处的实验现象。
(2)请用分子的观点解释B处颜色变化的原因。
(3)氨气在纯氧中燃烧的化学方程式是
 。把图乙中第三个方框补充完整。
。把图乙中第三个方框补充完整。
我要多选
作答:
答对了
答错了
根据下列实验回答问题:
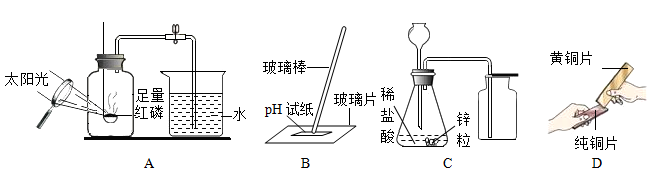
(1)A实验,用凸透镜聚光引燃红磷测定空气中氧气的含量,其优点是:______ 。
(2)B实验中,若玻璃片用水洗后没擦干,会导致待测稀硫酸的pH:______ 。
(3)C实验,用稀盐酸与锌反应制取氢气装置中的错误是:______ 。
(4)D实验中,黄铜片和纯铜片相互刻画,可观察到的现象是______ 。

(1)A实验,用凸透镜聚光引燃红磷测定空气中氧气的含量,其优点是:
(2)B实验中,若玻璃片用水洗后没擦干,会导致待测稀硫酸的pH:
(3)C实验,用稀盐酸与锌反应制取氢气装置中的错误是:
(4)D实验中,黄铜片和纯铜片相互刻画,可观察到的现象是

我要多选
作答:
答对了
答错了
我们的生活与化学密切相关。请回答:
(1)下列水的净化方法中净化程度最高的是_____(填字母序号)。(2)农村使用的泉水一般含有较多的钙、镁离子,属于硬水,可用______ 进行检验。
(3)健康人的体液必须维持在一定的酸碱度范围内,用______ 可以测定人体内或排出的液体的酸碱度,帮助我们了解身体健康状况。
(4)防止金属锈蚀是保护金属资源的有效措施之一。写一条防止铁制品生锈的常见方法:_____ 。
(5)每年全世界消耗大量的煤、_______ 、天然气等化石燃料,排放大量的二氧化碳,形成温室效应,导致气候异常,因此要节能减排。
(1)下列水的净化方法中净化程度最高的是_____(填字母序号)。(2)农村使用的泉水一般含有较多的钙、镁离子,属于硬水,可用
(3)健康人的体液必须维持在一定的酸碱度范围内,用
(4)防止金属锈蚀是保护金属资源的有效措施之一。写一条防止铁制品生锈的常见方法:
(5)每年全世界消耗大量的煤、
A.
静置沉淀
B.
吸附沉淀
C.
蒸馏
D.
过滤

我要多选
作答:
答对了
答错了
五、综合题
酸、碱、盐在生产和生活中有广泛的应用。
(1)用稀盐酸和氢氧化钙溶液进行中和反应实验时,反应过程中溶液pH变化曲线如图所示,请回答以下问题:
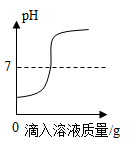
该实验操作是将____________ (写溶质的化学式)溶液逐滴加入另一种溶液中。当滴加到一定量并充分反应时,请对烧杯中溶质成分进行探究。
【提出问题】此时烧杯中的溶质成分是什么?
【猪想与假设】I:CaCl2Ⅱ:____________ Ⅲ:CaCl2和HCl
【实验与探究】
(2)为了除去粗盐中CaCl2、MgSO4等可溶性杂质,需进行如下操作:【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】
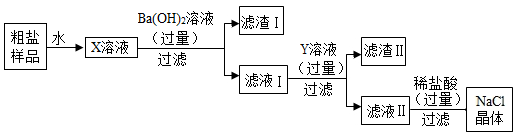
①写出加入Ba(OH)2时,发生反应的方程式__________ 。
②滤渣Ⅱ中的物质是什么?__________ (写化学式)
③请设计实验方案证明滤液Ⅱ中含有NaOH__________ 。(写出实验步骤和现象)
(3)100g某硫酸恰好与13g锌完全反应。试计算这种硫酸中溶质的质量分数。
(1)用稀盐酸和氢氧化钙溶液进行中和反应实验时,反应过程中溶液pH变化曲线如图所示,请回答以下问题:

该实验操作是将
【提出问题】此时烧杯中的溶质成分是什么?
【猪想与假设】I:CaCl2Ⅱ:
【实验与探究】
实验步骤 | 实验现象 | 实验结论 |
| 取少量上述烧杯中的溶液于试管中,向其中加入 | 猜想Ⅲ正确 |
(2)为了除去粗盐中CaCl2、MgSO4等可溶性杂质,需进行如下操作:【提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀;Na2CO3溶液呈碱性】

①写出加入Ba(OH)2时,发生反应的方程式
②滤渣Ⅱ中的物质是什么?
③请设计实验方案证明滤液Ⅱ中含有NaOH
(3)100g某硫酸恰好与13g锌完全反应。试计算这种硫酸中溶质的质量分数。

我要多选
作答:
答对了
答错了
某化学兴趣小组的同学为测定假黄金(铜锌合金)中锌的质量,取20克假黄金置于烧杯中,取120克稀盐酸,分6次加入,充分反应,实验数据如下:
请回答:
(1)表中m=_____ 。
(2)假黄金(铜锌合金)中锌的质量是_____ g。
(3)所用稀盐酸中溶质的质量分数是___ 。
(4)当恰好完全反应时,所得不饱和溶液中溶质质量分数为_____ ?(写出计算过程,计算结果保留0.1%)
(5)第6次实验结束后,最终溶液中溶质的化学式为_____ ,溶液的溶液pH____ (选填“>”“=”或“<”)7。
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量/g | 18.7 | 17.4 | m | 14.8 | 13.5 | 13.5 |
请回答:
(1)表中m=
(2)假黄金(铜锌合金)中锌的质量是
(3)所用稀盐酸中溶质的质量分数是
(4)当恰好完全反应时,所得不饱和溶液中溶质质量分数为
(5)第6次实验结束后,最终溶液中溶质的化学式为

我要多选
作答:
答对了
答错了
某公司生产的新型融雪剂,其成分是无水CaCl2和少量的NaCl,为测定CaCl2的含量,同学称取该样品12 g,加水充分溶解得到溶液50 g,然后取一定质量分数的Na2CO3溶液分五次加入,充分振荡,实验数据见表。请根据表格数据和图像信息完成下列问题:
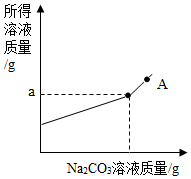
(1)X____ ,a=____ 。
(2)A点所示溶液的溶质为___ (填化学式),该溶液使无色酚酞溶液呈___ 色。
(3)样品中CaCl2的质量分数___ 。
(4)所用Na2CO3溶液的溶质质量分数___ 。
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入Na2CO3溶液的质量/g | 20 | 20 | 20 | 21 | 20 |
| 生成沉淀的质量/g | 2.5 | 5.0 | 7.5 | 10 | X |

(1)X
(2)A点所示溶液的溶质为
(3)样品中CaCl2的质量分数
(4)所用Na2CO3溶液的溶质质量分数

我要多选
作答:
答对了
答错了
声明:本文档由用户提供并上传,仅供用户内部交流学习使用,若内容存在侵权,请点击举报删除。
贡献者:
 Grace
Grace