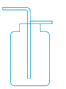

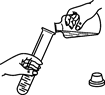





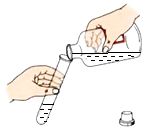
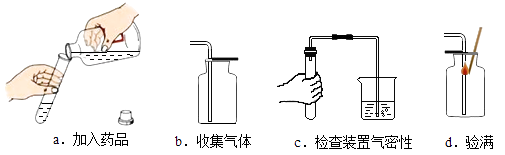
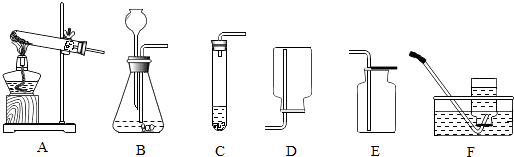
 加入药品
加入药品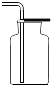 收集气体
收集气体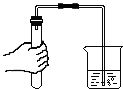 检查装置的气密性
检查装置的气密性




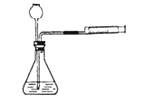



①不能用浓盐酸,因为浓盐酸易挥发,使氯化氢气体混入二氧化碳气体中 ②一般不选用碳酸钠粉末,因为它与酸反应的速率太快,不便于收集 ③可用木炭和氧气反应,因为反应可生成二氧化碳 ④可用稀盐酸与石灰石反应,因为反应的速度适中,条件要求不高,气体产物纯净,易于收集

请回答:

资料一:文献表明1体积水要完全溶解1体积二氧化碳,至少需要约7天的时间。如果是1天时间,则1体积水大约只能溶解  体积的二氧化碳。
体积的二氧化碳。
资料二:对任何气体的收集,凡能用排水法收集的气体,最好用排水法收集,这样既可以观察集气的快慢,又可以提高被收集气体的纯度。
资料三:二氧化碳不溶于饱和的碳酸氢钠溶液。

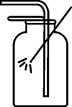
15℃、101kPa 下,1 体积水约能溶解 1 体积的二氧化碳,A 和 B 中质地较软的塑料瓶容积相等,装置的气密性良好,且充满 CO2。将 A 的瓶盖打开,加入体积约为塑料瓶容积 1/3 的蒸馏水,迅速旋紧瓶盖后充分振荡;向 B 中也注入体积约为塑料瓶容积 1/3 的蒸馏水,充分振荡。
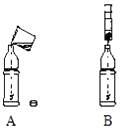
①A 中观察到的实验现象是________,其原因是________。
②B 中观察到的实验现象是________,其原因是________。



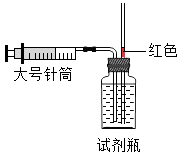
①用大号针筒抽取200毫升二氧化碳气体。
②向试剂瓶中加入200毫升水(恰好加满),塞紧双孔橡皮塞。
③连接大号针筒和试剂瓶,缓慢推动活塞,将二氧化碳注入水中。
推动活塞时应尽量缓慢,其目的是_________ 。

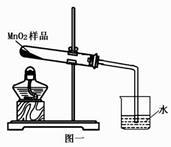
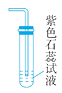
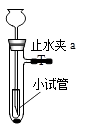
【假设 1】甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
实验步骤及现象 | 结论 |
_________ | 假设不成立。 |
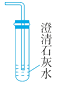
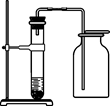
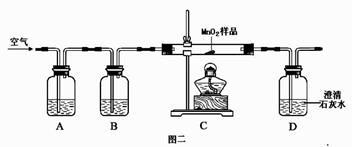
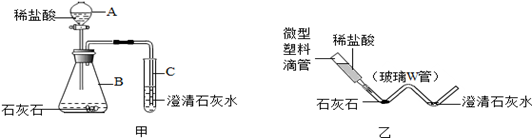
【假设2】乙同学认为:二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。他设计了如图二所示的实验进行研究,其中 B 装置的作用是检验 A 中反应是否完全,B中的试剂是_________,实验中乙同学从装置左端通入空气的目的是_________,结果观察到 D 处澄清石灰水变浑浊。他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现 D 处澄清的石灰水也变浑浊。


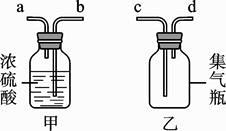
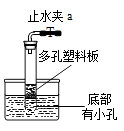
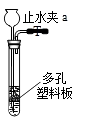
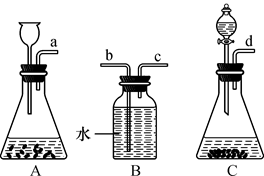
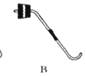
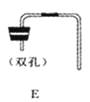
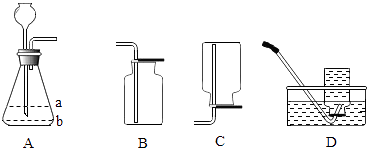
若要制取二氧化碳,在B装置中装有石灰石,那么a中应加入_________.若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放 _________ (填写试剂名称).如果用E装置收集该气体,则气体从_________端进入(填“b”或“c”).
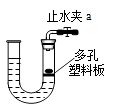
实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是_________.


请你回答下列问题:
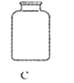
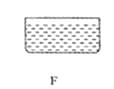
制取二氧化碳气体所需的药品是_________;
制取并收集二氧化碳气体所需的仪器是(用仪器的序号回答)_________;
收集二氧化碳气体的方法是_________;
检验二氧化碳气体是否收集满的方法是_________。

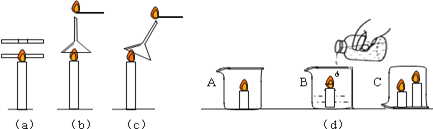
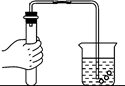
点燃一支蜡烛,观察到的现象有_________,其中发生的物理变化是_________.
先用一木筷迅速插入蜡烛火焰中,片刻后取出,观察到木筷表面出现了如图(a)上所示的圆弧状焦黑斑,其产生的原因是_________.
如图(b),在火焰正上方罩一个普通漏斗,用一燃着的火柴接近漏斗颈口处,可观察到火焰_________,是由于_________.(c)斜插入蜡烛焰心时,观察到漏斗颈口处产生了黄色火焰,这是由于_________.
如图(d),他在B烧杯中先加入适量的碳酸钠粉末,分别点燃四支蜡烛,然后在B杯中加入稀盐酸,(碳酸钠与稀盐酸反应能产生二氧化碳气体)将C烧杯倒罩在高矮不同的两支蜡烛上.在A、B两烧杯中,蜡烛先熄灭的是_________,是由于_________.C烧杯中先熄灭的是_________,是由于_________.

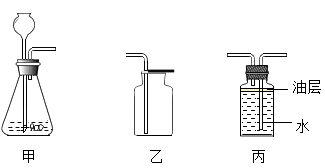

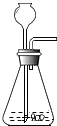
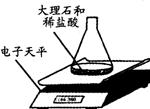
制取二氧化碳气体时,锥形瓶内液体应加至_________(选填“a”或“b”)处.
收集二氧化碳气体应选用的装置是_________.

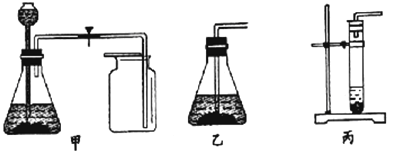
如图甲是实验室制取CO2的装置,实验中收集集满一瓶CO2后,应将盖有玻璃片的集气瓶_________(选填“正放”或“倒放”)在桌面上.
有两位同学对图甲中的气体发生装置进行了简化,简化后的装置如图乙和图丙所示,其中可行的是_________.


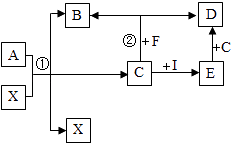
反应①:_________;
反应②:_________.

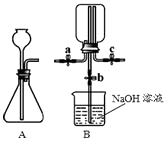
连接AB装置时,应将A装置中的导管连接B装置中的_________(选填a或c)。
连接完毕后,实验步骤如下:
①在A装置的锥形瓶中加入大理石,向长颈漏斗中注入稀盐酸。
②打开a、c,关闭b,向B中集气瓶内充入气体。检验集气瓶中气体已收集满的方法是_________。
③关闭a、c,打开b,用冷毛巾捂住B中集气瓶,一段时间后,观察到B装置中烧杯内液面下降,请解释原因_________。

甲:石灰石  CO2
CO2
乙:大理石  CO2
CO2
丙:碳酸钠  CO2
CO2

A.石灰石和稀硫酸反应制取CO2
B.大理石与稀盐酸反应制取CO2
C.锌粒与稀硫酸混合制取氢气.




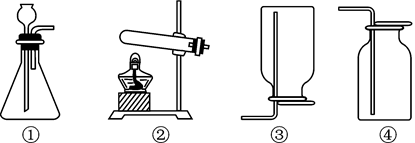
A、① B、② C、⑤ D、________.

请回答:


①将一定量的蛋壳放人容器中;②往其中加入适量的稀盐酸,观察到有较多的气泡产生;③……;④得出结论:蛋壳的主要成分是碳酸盐(如:碳酸钙)。
|
蛋壳的质量/克 |
加入稀盐酸质量/克 |
收集到CO2气体体积/升 |
|
7.5 |
100 |
1.1 |
假设二氧化碳全部是由蛋壳中的碳酸钙与盐酸反应产生,小明计算这些蛋壳中碳酸钙的质量分数的过程如下:
解:设该蛋壳中碳酸钙的质量为x
| CaCO3+2HCl=CaCl2+H2O+ | 2CO2↑ |
| 100 | 28 |
| x | 1.1升 |
100:28=x:1.1升
x=3.93,
蛋壳中碳酸钙的质量分数  =0.524
=0.524
小明的计算过程中存在明显错误,请你通过列式进行计算(保留1位小数)。

| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 大理石碎屑生成的 CO2 质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
| 块状大理石生成的 CO2 质量/克 | 0 | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |


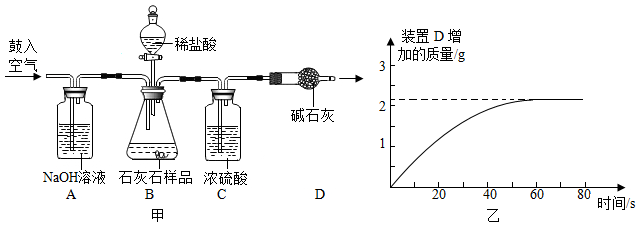
①去掉装置A,将空气直接鼓入装置B
②去掉装置C,将B与D装置直接相连
③当气泡停止产生时立即停止鼓入空气