以下为铝材表面处理的一种方法:
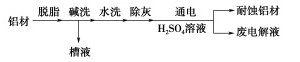
以铝材为阳极,在H2SO4溶液中通电,铝材表面形成氧化膜,阳极电极反应式为 。
对金属制品进行抗腐蚀处理可延长其使用寿命。
以下为铝材表面处理的一种方法:

以铝材为阳极,在H2SO4溶液中通电,铝材表面形成氧化膜,阳极电极反应式为 。
镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 。
利用如图装置可以模拟铁的电化学防护。
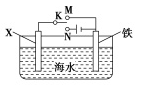
若X为碳棒,为减缓铁的腐蚀,开关K应置于 _处。若又为锌,开关K置于M处,该电化学保护法称为 。

如图所示,将拴有金属条的铁钉插在含有酚酞的NaCl溶液中,可以看到靠近金属条的溶液出现粉红色。则该金属条可能是( )
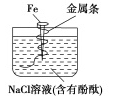
锌

我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象在铁帽上加锌环能有效防止铁帽的腐蚀,防护原理如图所示。
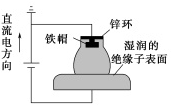
下列说法错误的是( )
通电时,锌环为阳极,发生氧化反应
通电时,阴极上的电极反应:2H2O+2e-=H2↑+2OH-
断电时,锌环上的电极反应: Zn2++2e-= Zn
断电时,仍能防止铁帽被腐蚀

一定条件下,碳钢腐蚀与溶液pH的关系如下表
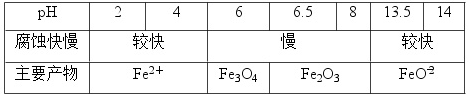
下列说法错误的是( )
当pH>14时,正极反应式:O2+4H++4e-=2H2O
在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会诚缓

家用炒菜锅用水清洗放置后,会出现红棕色的锈斑。在此变化过程中不可能发生的化学反应是( )
4Fe(OH)2+2H2O+O2=4Fe(OH)3
2Fe+2H2O+O2=Fe(OH)2
正极反应式:2H2O+O2+4e-=4OH-
负极反应式:Fe-3e-=Fe3+

钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量 的四分之一。请回答下列问题:
钢铁腐蚀主要是吸氧腐蚀,写出该腐蚀过程中的电极反应式:
负极 ,
正极 。
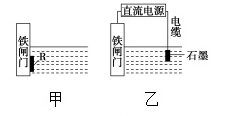
为了降低某水库的铁闸门的腐蚀速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用 (填序号)。
铜
钠
锌
石墨
图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的 极上。

生铁在pH=2和pH=4的盐酸中发生腐蚀。在密闭容器中,用压强传感器记录该过程的压强变化,如图所示。下列说法中不正确的是( )
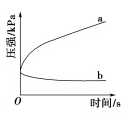
两容器中负极反应均为Fe-2e- =Fe2+
曲线a记录的是pH=2的盐酸中压强的变化
曲线b记录的容器中正极反应是O2+4e-+2H2O=4OH-
在弱酸性溶液中,生铁能发生吸氧腐蚀

某城市为了减少钢管因锈蚀而造成的损失,拟用如图所示方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )
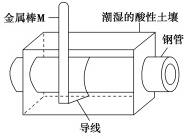
在潮湿的酸性土壤中H+向金属棒M移动,抑制H+与铁的反应
钢管与金属棒M也可用导线分别连接直流电源正、负极以达到减缓腐蚀钢管的目的

为探究钢铁的吸氧,腐蚀原理,设计了如图所示的装置,下列有关说法中错误的是( )
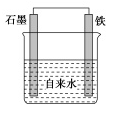
正极的电极反应式为O2+2H2O+4e-=4OH- 1
将石墨电极改成Mg电极,难以观察到铁锈生成
若向自来水中加入少量NaCl(s),可较快地看到铁锈
分别向铁、石墨电极附近吹入O2,前者铁锈出现得快

关于铁生锈的机理有人提出如下4个步骤:
①Fe-2e-=Fe2+ ②H++e-=H ③4H+O2=2H2O ④4Fe2++O2+(4+2x)H2O=2Fe2O·xH2O+8H+
试根据以上过程回答下列问题:
根据以上机理,判断下列说法正确的是 (填序号,下同)。
A.以上锈蚀过程发生的是化学腐蚀
B.从锈蚀反应的最终结果看,水既是氧化剂,又是还原剂
C.反应的实质是氧气被还原,金属铁被氧化
D.从反应机理看,锈蚀过程发生的是析氢腐蚀
某铁件需长期浸于水下,为了减缓腐蚀,采取的下列措施正确的有 。
A.给铁件铆上一些锌板
B.给铁件通入直流电,把铁件与电源正极连接
C.在制造铁件时,在铁中掺入一定比例的铜制成合金
D.在铁件表面涂上一层较厚的沥青
质量为1000g的某铁件已在水下生锈,若已知整个锈蚀过程中有6mol电子发生转移,则参加反应的O2在标准状况下的体积为 L,生锈后铁件的质量为 g(已知铁锈Fe2O·xH2O中x的值为1)。

下列表面上镀有金属保护层的铁板中,当镀层破损后,在相同条件下最不易被腐蚀的是( )
镀锌铁板
镀锡铁板
镀银铁板
镀铜铁板

(双选)下列有关金属电化学腐蚀的说法中正确的是( )
吸氧腐蚀比析氢腐蚀普遍

某研究小组对铁生锈的条件进行探究。请回答下列问题:
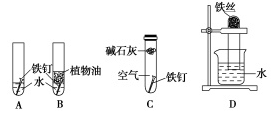
甲同学设计了A、B、C一组实验(如图所示),探究铁生锈的条件。经过较长时间后,甲同学观察到A中铁钉生锈;B中铁钉不生锈;C中铁钉不生锈。
①通过分析上述实验现象,可得出铁生锈的外部条件是 ;
②铁钉发生电化学腐蚀的正极反应式为 ;
③实验B所用的水要经过 处理,植物油的作用是 。
④实验C中碱石灰的作用是 。
乙同学设计了实验D(如图所示),一段时间后,发现试管中的液面升高,其原因是 。

为了避免青铜器生成铜绿,下列方法中正确的是( )
①将青铜器放在银质托盘上 ②将青铜器保存在干燥的环境中 ③将青铜器保存在潮湿的空气中 ④在青铜器的表面覆盖一层防渗的高分子膜
①③
①④

由图分析,下列叙述正确的是( )
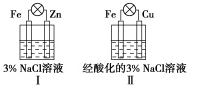
I和II中正极均被保护
I和II中C1-均向Fe电极移动
I和II中负极反应均是Fe-2e-= Fe2+
I和II中正极反应均是O2+4e-+2H2O=4OH-

在下列各种情况下,埋在地下的输油铸铁管道的腐蚀速率最慢的是( )
在潮湿疏松的酸性土壤中
在潮湿疏松透气的土壤中
在干燥致密不透气的土壤中
在含碳较多、潮湿透气的土壤中