原子半径:Y>Z>R>T
被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种主族元素组成,其化学式为X3Y2(ZWR4)3T2,其中X、Y、Z为金属元素Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层电子数的3倍,T无正价又与R原子序数之和是W的2倍。下列说法错误的是( )
气态氢化物的稳定性:W<R<T
最高价氧化物对应的水化物的碱性:X>Z
XR2、WR2两种化合物中R的化合价相同

下表分别是含元素X、Y的物质性质的比较及得出的结论,其中结论不正确的是( )

A
B
C
D

a、b、c、d为1~18号元素a的原子中只有1个电子,b2+和c+的电子层结构相同,d与b最外层电子数相同。下列叙述错误的是( )
a与其他三种元素形成的二元化合物中其化合价均为-1

114号元素符号为Fl,名称为“鈇”,这是为了纪念苏联原子物理学家乔治·弗洛伊洛夫。 以下对“鈇”的叙述正确的是( )
它是一种非金属元素
主要化合价为-4价、+4价
位于元素周期表的第七周期

W、X、Y、Z是原子序数依次增大的短周期主族元素,W的氢化物水溶液能刻蚀玻璃,X、Y 处于相邻位置,Y的最高化合价与最低化合价的代数和为零,W、X原子的最外层电子数之和与 Y、Z原子的最外层电子数之和相等。下列说法错误的是( )
简单离子的电子层结构:W与X相同

元素周期表是学习化学的重要工具,它隐含着许多信息和规律。下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm)。

用元素代号标出它们在周期表中对应位置(以下为周期表的一部分)
B元素处于周期表中 周期 族;
B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为 ;
上述五种元素的最高价氧化物对应水化物中酸性最强的是 (填化学式);
C、E形成的化合物为 (填化学式)。

下列说法正确的是( )
原子核外最外层电子数相同的元素族数一定相同
同一主族的元素最高化合价一定相同

无机化学命名委员会在1989年作出决定,把长式元素周期表原先的主、副族及族号取消,由左到右改为18列.按此规定,下列说法中错误的是( )
第15列元素的最高价氧化物的化学式是R2O3
第17列元素单质熔、沸点逐渐升高
第11列中肯定没有非金属元素
在18列元素中,第3列的元素种类最多

某元素x的原子序数为52,下列叙述正确的是( )
X的最高价氧化物对应水化物的酸性比HBrO4的酸性强
X形成的气态氢化物比H2S稳定澈
x原子的得电子能力比碘原子的得电子能力强
x的主要化合价是-2、+4、+6

表中①~⑥为短周期元素及相应部分原子半径的数据。下列说法正确的是( )
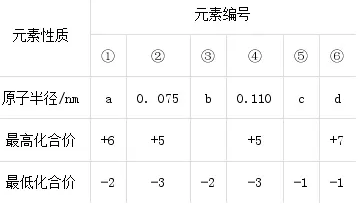
元素①的最外层电子排布为2s22p4
元素②氢化物与元素⑥氢化物反应形成化合物中只有共价键
原子半径:a>d>b>c
非金属性:元素⑥>元素④>元素①

砷为第四周期ⅤA族元素,依据它在周期表中的位置,推测砷不可能具有的性质是( )
砷的最高价氧化物的水化物砷酸(H2AsO4)的酸性比磷酸(H3PO4)弱
砷化氢(AsH3)不稳定,还原性比氨NH3弱

如果发现了原子序数为116的元素,下列对它的叙述中正确的是( )
①位于第7周期
②非金属元素
③最外电子层有6个电子
④没有放射性
⑤属于氧族元素
⑥属于锕系元素
①③⑤
②④⑥
①③⑥
③④⑤

如表为几种短周期元素的性质:
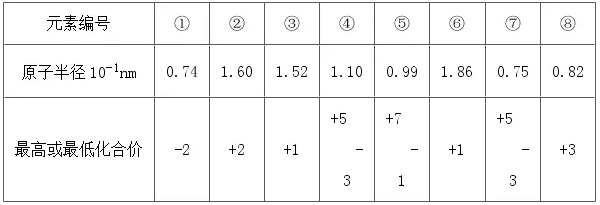
对上述元素有关说法正确的是( )
元素④的原子序数小于元素⑦的原子序数
②、⑧处于同一周期
上述八种元素中,最高价氧化物对应水化物酸性最强的元素是⑤
⑧号元素原子结构示意图:

根据泡利的原子轨道能级图和“能级交错”现象,原子轨道的能量高低顺序是:ns<(n-3)g<(n-2)f<(n-1)d<np(n为能层序数,g能级中有9个轨道)。则未来的第八周期应包括的元素的种类是( )
32
50
64
128

下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )

A、B的单质与稀盐酸反应速率B>A
D、E形成的简单离子的还原性E>D
气态氢化物的稳定性HD<H2C
最高价氧化物对应的水化物的酸性H2CO4>HEO4

五种短周期元素X、Y、Z、M、w的原子序数与其常见化合价的关系如图所示,下列关系不正确的是( )
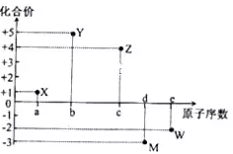
X2W中各原子均达8电子稳定结构
元素气态氢化物的稳定性:YH3>MH3

如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
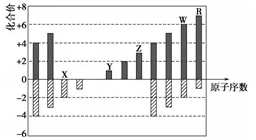
原子半径:Z>Y>X
气态氢化物的稳定性:R<W
WX3和水反应形成的化合物是离子化合物
Y和Z两者最高价氧化物对应的水化物能相互反应

2016年6月,国际纯化学和应用化学联合会(IUPAC)将新发现的四个新元素(113号、115号、117号、118号)加入到元素周期表中.至此这一周期元素全部排满。下列关于第七周期元素的推论错误的是( )
第七周期排满时有32种元素
第七周期排满时最后一种单质不与任何物质发生化学反应
第七周期第ⅦA族元素原子序数117,是一种金属元素
第七周期第ⅢA族元素的氢氧化物具有较强的碱性

如图所示,已知A元素的最低化合价为-3,它的最高价氧化物含氧56.34%原子核内中子数比质子数多1。试回答:

写出它们的元素符号:A ,B ,C ,D ,E .
A、B、C、D的气态氢化物稳定性最差的是 .
A、B、C的原子半径由小到大的顺序是 .
A、B、C三元素最高价氧化物对应水化物的酸性由强到弱的顺序是 .

W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如下图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。
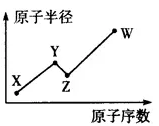
请回答下列问题:
写出四种元素的元素符号:
W ;X ;Y ;Z .
四种元素的所有化合价中,最低负化合价为 价.最高正化合价为 价。
甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有消毒杀菌作用,其化学式为 ;化合物乙是一种常见的化肥,其化学式为 .
HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确,说明理由: .