







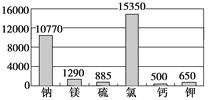
材料1:下图为海水中各元素含量情况(mg/L)
材料2:部分化学试剂的市场价格
试剂 | 氢氧化钾 | 氢氧化钠 | 氢氧化钙 | 氧化钙 |
价格(元/吨) | 5238.0 | 2300.00 | 1200.00 | 700.00 |
请回答下列问题:
在海水提镁的过程中要实现对镁离子的富集、分离,有以下三个方案:
方案一:直接往海水中加入沉淀剂;
方案二:加热蒸发海水后再加入沉淀剂;
方案三:在晒盐后的卤水中加入沉淀剂。
你认为方案_________最合理。
不选方案_________的理由是_________。
不选方案_________的理由是_________。
应该选择_________试剂作为镁离子的沉淀剂。不考虑其他费用,沉淀相同量的镁离子所用氢氧化钠和氧化钙的价格比为_________。
为了节省成本,你可考虑以海边上的贝壳为原料,试简述其理由:?

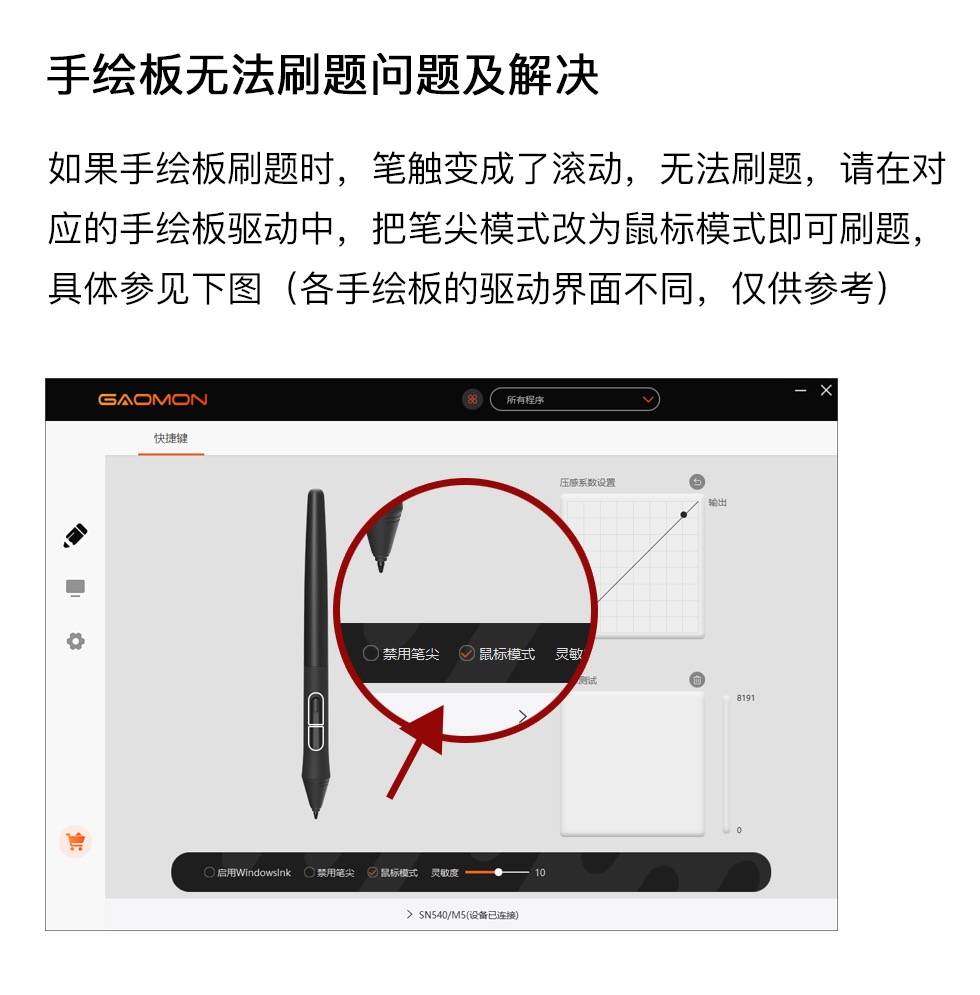
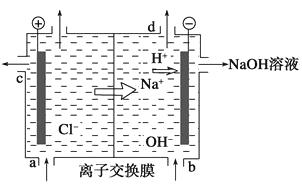
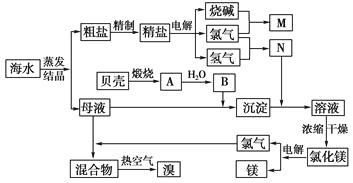
电解饱和食盐水常用离子膜电解槽和隔膜电解槽,离子膜和隔膜共同允许通过的分子或离子是_________,电解槽中的阳极材料为_________。
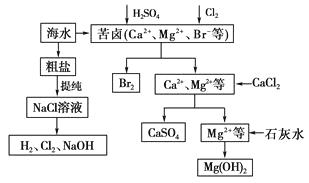
本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备?_________,原因是_________。
溴在四氯化碳中的溶解度比在水中大得多,四氯化碳与水不互溶,但在上述工艺中却不用四氯化碳,原因是_________。


请回答:
Mg(OH)2中加入盐酸后,要获得MgCl2·6H2O晶体,需要进行的实验操作依次为_________。
A.蒸馏
B.灼烧
C.过滤
D.蒸发
E.冷却结晶
利用MgCl2·6H2O可制得无水氯化镁,应采取的措施是_________。
目前工业上主要采用隔膜法电解饱和食盐水,下列关于隔膜电解槽的叙述错误的是________。
母液中常含有MgCl2、NaCl、MgSO4,KCl等,可进一步加工制得一些重要的产品。若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是_________;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的_________晶体。
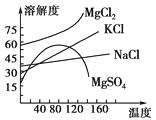

从离子反应的角度思考,在母液中加入石灰乳所起的作用是?
石灰乳是生石灰与水作用形成的化合物,从充分利用当地海洋化学资源,提高生产与经济效益的角度考虑,生产生石灰的主要原料是?
电解熔融的无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是(填写代号):( )